肝臓・胆道・膵臓:臨床研究についてComparative analysis of preoperative nutrition & inflammatory marker in borderline and resectable pancreatic cancer patients [Neoadjuvant treatment vs upfront surgery patients]
(切除可能膵癌および切除可能境界膵癌患者における、術前の栄養および炎症性マーカーの比較分析 [術前化学療法と手術先行患者における比較])
Comparative analysis of preoperative nutrition & inflammatory marker in borderline and resectable pancreatic cancer patients [Neoadjuvant treatment vs upfront surgery patients]
(切除可能膵癌および切除可能境界膵癌患者における、術前の栄養および炎症性マーカーの比較分析 [術前化学療法と手術先行患者における比較])
1.臨床研究について
当院では、最適な治療を患者さんに提供するために、病気の特性を研究し、診断法、治療法の改善に努めています。その一つとして、当院では、日本と韓国の施設で膵癌の手術を受けられた患者さんのデータを用いた「切除可能膵癌および切除可能境界膵癌患者における、術前栄養および炎症性マーカーの比較分析[術前化学療法と手術先行患者における比較]」を行っております。
今回の研究の実施にあたっては、日本側施設の代表である九州大学において、九州大学医系地区部局観察研究倫理審査委員会の審査を経て、研究機関の長より許可を受けています。この研究が許可されている期間は、2026年12月31日までです。
2.研究の目的や意義について
現在、膵癌の治療においては、術前に化学療法もしくは化学放射線療法を行って根治切除術を行うことが増えています。このような術前補助療法は、患者さんの栄養状態や、術後の治療成績に影響する可能性がありますが、具体的にどのような影響があるのか明らかになっておりません。そこで、本研究により、術前に補助療法を受けていない患者さんと、術前に補助療法を受けた患者さんの、血液検査による栄養学的指標と炎症性数値を解析し、術前補助療法が膵癌の治療成績に及ぼす影響を明らかにすることを目的としています。日本と韓国では、術前補助療法の適応に違いがあり、また手術前の栄養管理も異なることが予想されます。このような文化的・医学的背景の差異から、最適な術前治療を明らかにするのも本研究の目的になります。本解析により、補助療法を受ける患者さんにとって、術前の栄養サポートの必要性について明らかにすることを考えています。
3.研究の対象者について
本研究は、日本と韓国の病院で2018年1月1日から2020年12月31日までに通常型膵癌に対し根治的膵切除術を受けた18歳以上の患者さんおよそ2000人が対象です。研究の対象者となることを希望されない方又は研究対象者のご家族等の代理人の方は、事務局までご連絡ください。
4.研究の方法について
この研究を行う際は、各施設でカルテに保存されている以下の情報を取得し解析します。
〔取得する情報〕
(一般情報)
年齢(年)、性別、体重、身長、BMI、ASAスコア(表1)、飲酒歴、喫煙歴、高血圧、糖尿病、手術歴、その他の既往歴
(手術前の情報)
白血球数、好中球割合、リンパ球割合、Hb値、PLT値、AST値、ALT値、BUN値、Cr値、アルブミン値、総ビリルビン値、直接ビリルビン値、Na値、K値、コレステロール値、CRP値、PT-INR値、CEA値、CA19-9値、術前補助療法の有無、術前補助療法のレジメン、RECIST判定
(手術関連情報)
手術日、術式、手術時間、術中輸血、ドレナージの有無、門脈合併切除、複合手術の有無、術後有害事象(表2: Clavien-Dindo分類)、有害事象の治療法、在院死の有無、術後膵液瘻、胃内容排出遅延、術後出血、出血、腹水、敗血症、創傷合併症、心血管合併症、肺合併症、腎臓合併症、肝胆道合併症、ICU再入室、再手術、再手術の原因、院内死亡の原因、術後90日以内死亡、退院日
(病理学的情報)
組織型、T因子(Tis/T1/T2/T3/T4)、腫瘍径、組織学的分化度、摘出リンパ節数、転移性リンパ節数、リンパ管浸潤、神経周囲浸潤、R0 /R1切除
(長期成績に関する情報)
術後補助療法、補助化学療法のレジメン、補助放射線治療、再発の有無、再発部位、再発確認日、生死、最終生存確認日
表1:ASA術前状態分類

表2:Clavien-Dindo分類

共同研究機関の研究対象者の臨床情報についても、電子ファイルで収集し、詳しい解析を行う予定です。
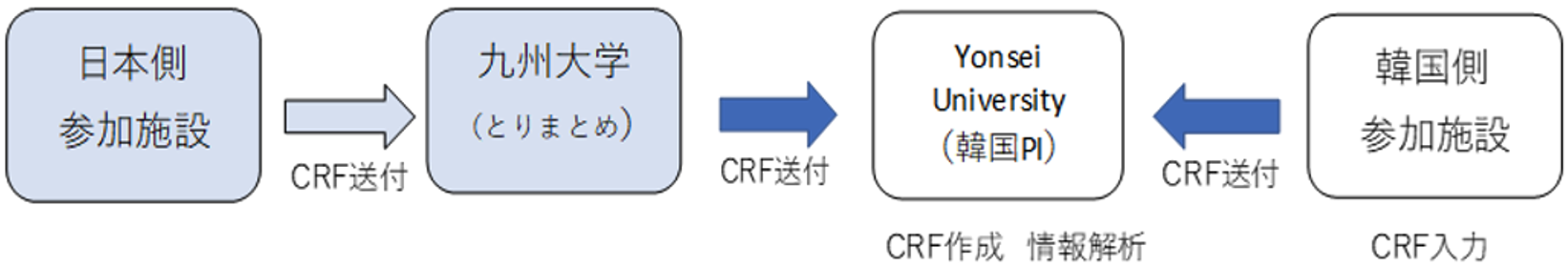
データの流れは下記の図のようになります。
※CRF:匿名化された情報
〔利用又は提供を開始する予定日〕
研究許可日以降
Yonsei Universityへ研究対象者の診療記録を九大のファイル共有システムにて送付し、詳しい解析を行う予定です。共同研究機関の研究対象者の診療記録についても、九大のファイル共有システムにて収集し、詳しい解析を行う予定です。他機関への試料・情報の送付を希望されない場合は、送付を停止いたしますので、ご連絡ください。
5.研究への参加を希望されない場合
この研究への参加を希望されない方は、下記の相談窓口にご連絡ください。
なお、研究への参加を撤回されても、あなたの診断や治療に不利益になることは全くありません。
その場合は、収集された情報は廃棄され、取得した情報もそれ以降はこの研究目的で用いられることはありません。ただし、すでに研究結果が論文などで公表されていた場合には、完全に廃棄できないことがあります。
6.個人情報の取扱いについて
研究対象者の測定結果、カルテの情報をこの研究に使用する際には、研究対象者のお名前の代わりに研究用の番号を付けて取り扱います。研究対象者と研究用の番号を結びつける対応表のファイルにはパスワードを設定し、九州大学大学院医学研究院 臨床・腫瘍外科学分野内のインターネットに接続できないパソコンに保存します。このパソコンが設置されている部屋は、同分野の職員によって入室が管理されており、第三者が立ち入ることはできません。また、本臨床情報は共同研究機関であるYonsei Universityに、匿名化された状態で送付され、本学と同様に厳重に管理されます。
また、この研究の成果を発表したり、それを元に特許等の申請をしたりする場合にも、研究対象者が特定できる情報を使用することはありません。
この研究によって取得した情報は、九州大学大学院医学研究院 臨床・腫瘍外科学分野・教授・中村雅史の責任の下、厳重な管理を行います。
ご本人等からの求めに応じて、保有する個人情報を開示します。情報の開示を希望される方は、ご連絡ください。
他機関に試料・情報を送付する場合
研究対象者のカルテの情報をYonsei Universityへ送付する際には、九州大学にて上記の処理をした後に行いますので、研究対象者を特定できる情報が外部に送られることはありません。
- 試料・情報の提供を行う国:大韓民国
- 大韓民国における個人情報の保護に関する制度に関する情報:
https://www.ppc.go.jp/enforcement/infoprovision/laws/offshore_report_korea/ - 上記、韓国個人情報保護法は我が国と同等水準のものではないが、一定の個人情報保護体制が整備されており、本研究に用いられる情報は厳重に管理されることになる。
7.試料や情報の保管等について
〔情報について〕
この研究において得られた研究対象者のカルテの情報等は原則としてこの研究のために使用し、研究終了後は、九州大学大学院医学研究院 臨床・腫瘍外科学分野において同分野教授・中村雅史の責任の下、10年間保存した後、研究用の番号等を消去し、廃棄します。
しかしながら、この研究で得られた研究対象者の情報は、将来計画・実施される別の医学研究にとっても大変貴重なものとなる可能性があります。そこで、前述の期間を超えて保管し、将来新たに計画・実施される医学研究にも使用させていただきたいと考えています。その研究を行う場合には、改めてその研究計画を倫理審査委員会において審査し、承認された後に行います。
8.この研究の費用について
この研究に関する必要な費用は、日本肝胆膵外科学会プロジェクト研究 研究費でまかなわれます。
9.利益相反について
当院では、よりよい医療を社会に提供するために積極的に臨床研究を推進しています。そのための資金は公的資金以外に、企業や財団からの寄付や契約でまかなわれることもあります。医学研究の発展のために企業等との連携は必要不可欠なものとなっており、国や大学も健全な産学連携を推奨しています。
一方で、産学連携を進めた場合、患者さんの利益と研究者や企業等の利益が相反(利益相反)しているのではないかという疑問が生じる事があります。そのような問題に対して九州大学では「九州大学利益相反マネジメント要項」及び「医系地区部局における臨床研究に係る利益相反マネジメント要項」を定めています。本研究はこれらの要項に基づいて実施されます。
本研究に関する必要な経費は日本肝胆膵外科学会プロジェクト研究 研究費を使用する予定であり、研究遂行にあたって特別な利益相反状態にはありません。
10.研究に関する情報の開示について
この研究に参加してくださった方々の個人情報の保護や、この研究の独創性の確保に支障がない範囲で、この研究の研究計画書や研究の方法に関する資料をご覧いただくことができます。資料の閲覧を希望される方は、ご連絡ください。
この研究では、学会等への発表や論文の投稿により、研究成果の公表を行う予定です。11.特許権等について
この研究の結果として、特許権等が生じる可能性がありますが、その権利は九州大学及び共同研究機関等に属し、あなたには属しません。また、その特許権等を元にして経済的利益が生じる可能性がありますが、これについてもあなたに権利はありません。
12.研究を中止する場合について
研究責任者の判断により、研究を中止しなければならない何らかの事情が発生した場合には、この研究を中止する場合があります。なお、研究中止後もこの研究に関するお問い合わせ等には誠意をもって対応します。
13.研究の実施体制について
この研究は以下の体制で実施します。
研究実施場所 |
九州大学大学院医学研究院臨床・腫瘍外科学分野 |
|
研究責任者 |
九州大学病院胆道・膵臓・膵臓移植・腎臓移植外科 講師 池永直樹 |
|
研究分担者 |
九州大学大学院医学研究院臨床・腫瘍外科学分野 教授 中村雅史 |
|
共同研究機関等 |
機関名 / 研究責任者の職・氏名・(機関の長名) |
役割 |
自治医科大学 消化器一般移植外科 教授 佐田尚宏(病院長 川合謙介) |
情報の収集・提供 |
|
14.相談窓口について
この研究に関してご質問や相談等ある場合は、下記までご連絡ください。
なお、この研究に関するすべてのお問い合わせも下記で受け付けます。
[お問い合わせ先]
近畿大学医学部 外科学教室 肝胆膵部門 助教 阿見 勝也
電話:072-366-0221(内線:6786)
近畿大学医学部での研究責任者:
近畿大学医学部 外科学教室 肝胆膵部門 主任教授 松本 逸平
【留意事項】
本研究は九州大学医系地区部局観察研究倫理審査委員会において審査・承認後、以下の研究機関の長(試料・情報の管理について責任を有する者)の許可のもと、実施するものです。
九州大学病院長 中村 雅史